นิยามและความสำคัญของปัญหา ED
ภาวะหย่อนสมรรถภาพทางเพศ (Erectile Dysfunction – ED) หมายถึงภาวะที่อวัยวะเพศชายไม่สามารถแข็งตัวหรือคงการแข็งตัวได้อย่างเพียงพอในขณะที่มีเพศสัมพันธ์ ปัญหานี้พบได้บ่อยในผู้ชาย เพิ่มขึ้นตามอายุ – มีรายงานการศึกษาว่าผู้ชายอายุประมาณ 40 ปีราว 40% เคยประสบภาวะ ED และตัวเลขนี้เพิ่มเป็นประมาณ 70% ในช่วงอายุ 70 ปี งานวิจัยจากสหรัฐอเมริกาพบว่าผู้ชายวัยกลางคน (40-70 ปี) กว่า 52% มีความผิดปกติด้านการแข็งตัวในระดับใดระดับหนึ่ง ปัจจุบันนี้คาดการณ์ว่าในปี ค.ศ.2025 จะมีจำนวนผู้ชายทั่วโลกที่ประสบภาวะ ED สูงถึง 322 ล้านคน ซึ่งสะท้อนให้เห็นว่า ED เป็นปัญหาสาธารณสุขที่สำคัญระดับโลก ไม่ใช่แค่เรื่องเฉพาะบุคคล
ความสำคัญของ ED ไม่ได้จำกัดอยู่เพียงปัญหาทางเพศเท่านั้น แต่ยังเชื่อมโยงกับสุขภาพโดยรวม. ED อาจเป็น สัญญาณเบื้องต้นของโรคหัวใจและหลอดเลือด – มีข้อมูลว่าเกือบ 50% ของผู้ชายที่มีโรคหลอดเลือดหัวใจ (Coronary artery disease) ตรวจพบว่ามีภาวะ ED ร่วมด้วย และ ED มักเกิดขึ้นนำหน้าการวินิจฉัยโรคหัวใจหลายปี (เฉลี่ย 3-5 ปี) การวิเคราะห์กลุ่มตัวอย่างขนาดใหญ่ (กว่า 90,000 คน) ยังพบว่าผู้ชายที่มี ED มีความเสี่ยงเกิดเหตุการณ์หัวใจและหลอดเลือด (เช่น กล้ามเนื้อหัวใจตายหรือโรคหลอดเลือดสมอง) สูงกว่ากลุ่มที่ไม่มี ED อย่างมีนัยสำคัญ (เพิ่มขึ้นประมาณ 40-50%) ดังนั้น ED จึงถือเป็นตัวบ่งชี้ภาวะสุขภาพที่สำคัญ – การพบ ED ในผู้ชายวัยกลางคนควรให้แพทย์ประเมินปัจจัยเสี่ยงโรคหัวใจและโรคเรื้อรังอื่นๆ ด้วย
นอกจากนี้ ED ยังส่งผลต่อคุณภาพชีวิตและสุขภาพจิตของผู้ป่วยอย่างมาก แม้ว่าสาเหตุหลักของ ED ในหลายกรณีจะมิได้เกิดจากปัญหาจิตใจโดยตรง แต่การที่ผู้ชายเกิดภาวะนี้ ย่อมบั่นทอนความเชื่อมั่นในตนเอง ก่อให้เกิดความเครียด วิตกกังวล และทำให้ความสัมพันธ์กับคู่นอนตึงเครียดได้ ผู้ป่วย ED จำนวนมากและคู่ครองของพวกเขามักเกิดความทุกข์ใจทางอารมณ์อย่างมีนัยสำคัญ และรู้สึกว่าคุณภาพชีวิตลดลงจากปัญหาการแข็งตัวของอวัยวะเพศที่เกิดขึ้น ด้วยเหตุนี้ การรักษา ED ให้ได้ผลไม่เพียงแต่ช่วยฟื้นฟูสมรรถภาพทางเพศ แต่ยังช่วยฟื้นฟูสุขภาวะทางจิตใจและความสัมพันธ์ของผู้ป่วยอีกด้วย
สาเหตุของภาวะหย่อนสมรรถภาพทางเพศ
สาเหตุของ ED มีความหลากหลายและมักเป็น หลายปัจจัยร่วมกัน (multifactorial). โดยทั่วไปสามารถแบ่งออกเป็นปัจจัยทางกาย (organic causes) และปัจจัยทางจิตใจ (psychogenic) รวมถึงปัจจัยเสี่ยงด้านพฤติกรรมและโรคร่วมอื่นๆ:
-
สาเหตุทางกายภาพ: กลุ่มนี้พบได้บ่อยในผู้ชายวัยกลางคนและสูงอายุ และประกอบด้วยหลายระบบของร่างกาย ได้แก่ ปัจจัยหลอดเลือด (vasculogenic) เช่น ภาวะหลอดเลือดแดงแข็ง (atherosclerosis) ความดันโลหิตสูง โรคหลอดเลือดหัวใจ และภาวะที่ส่งผลต่อการไหลเวียนเลือดไปเลี้ยงองคชาต (ED จากหลอดเลือดคิดเป็นสัดส่วนสูงที่สุดของ ED ทางกาย); ปัจจัยเมตาบอลิกและต่อมไร้ท่อ เช่น โรคเบาหวานชนิดที่ 2, ภาวะอ้วน, กลุ่มอาการเมตาบอลิก และภาวะฮอร์โมนเพศชายต่ำ (hypogonadism) หรือความผิดปกติของไทรอยด์ ซึ่งสามารถรบกวนกลไกการแข็งตัวได้ในระดับโมเลกุล ปัจจัยทางระบบประสาท เช่น โรคทางระบบประสาท (โรคพาร์กินสัน, เส้นเลือดสมองตีบ), การบาดเจ็บไขสันหลัง, เส้นประสาทส่วนปลายเสียหาย (เช่น จากเบาหวาน) หรือโรคปลอกประสาทเสื่อมแข็ง (multiple sclerosis) ล้วนสามารถรบกวนการส่งสัญญาณประสาทที่กระตุ้นการแข็งตัว; ปัจจัยทางกายวิภาคหรืออุบัติเหตุ เช่น การบาดเจ็บที่อุ้งเชิงกรานหรือองคชาต การผ่าตัดต่อมลูกหมาก (เช่น การผ่าตัดมะเร็งต่อมลูกหมาก) หรือการฉายรังสีในบริเวณอุ้งเชิงกราน ล้วนเป็นสาเหตุให้เกิดความเสียหายต่อเส้นเลือดหรือเส้นประสาทที่ไปเลี้ยงองคชาต; ยาและสารบางชนิด: ยาหลายประเภทสามารถส่งผลข้างเคียงทำให้เกิด ED ได้ เช่น ยากลุ่มลดความดันโลหิต (โดยเฉพาะยาขับปัสสาวะและเบต้า-บล็อกเกอร์), ยาต้านเศร้าและยาจิตเวชบางชนิด, ยารักษาโรคต่อมลูกหมาก (เช่น ยา finasteride), ยาเสพติด (แอลกอฮอล์, สารเสพติด) การสูบบุหรี่จัดและการปั่นจักรยานทางไกลเป็นเวลานาน (ทำให้เกิดแรงกดทับเส้นเลือด/เส้นประสาทบริเวณฝีเย็บ) ก็เป็นปัจจัยเสี่ยงทางกายอีกประการหนึ่งของ ED
-
สาเหตุทางจิตใจ: ปัจจัยด้านจิตใจหรืออารมณ์สามารถก่อให้เกิดหรือซ้ำเติม ED ได้ แม้ในกรณีที่มีสาเหตุทางกายร่วมด้วย. ภาวะ ความเครียดและวิตกกังวลเกี่ยวกับการแสดงออกทางเพศ (performance anxiety) เป็นสาเหตุจิตใจที่พบได้บ่อย โดยเฉพาะในผู้ชายอายุน้อยที่เพิ่งเริ่มมีเพศสัมพันธ์หรือมีประสบการณ์ล้มเหลวครั้งก่อน. โรคซึมเศร้า และความผิดปกติทางอารมณ์อื่นๆ สามารถลดความต้องการทางเพศและขัดขวางกระบวนการกระตุ้นการแข็งตัวผ่านกลไกทางประสาทเคมี ปัญหาความสัมพันธ์ระหว่างคู่ครอง (เช่น ความขัดแย้ง, ความเบื่อหน่ายทางเพศ, การขาดความสนใจหรือความไว้วางใจ) ล้วนมีผลทางอ้อมให้เกิด ED ทางจิตใจได้. ผู้ชายที่เผชิญแรงกดดันทางอาชีพหรือชีวิตประจำวันสูง, นอนหลับพักผ่อนไม่เพียงพอ, หรือมีภาพลักษณ์ตนเองที่ไม่ดี (เช่น รู้สึกว่าตนเองไม่ดึงดูด) ก็อาจประสบปัญหา ED ชั่วคราวได้จากปัจจัยทางจิตเหล่านี้
-
ปัจจัยผสมผสานและโรคร่วม: ในผู้ป่วยจำนวนมาก ED มักเกิดจากหลายปัจจัยร่วมกัน ทั้งทางกายและจิตใจ. ตัวอย่างเช่น ผู้ป่วยเบาหวาน (ปัจจัยกาย) อาจมีความวิตกกังวลเรื่องสมรรถภาพ (ปัจจัยจิตใจ) ร่วมด้วย – ทั้งสองส่วนนี้ส่งผลต่อกันและทำให้ ED รุนแรงขึ้น. อายุที่มากขึ้น ก็เป็นปัจจัยเสริมที่สำคัญต่อ ED โดยทางอ้อม ผ่านการเพิ่มโอกาสเกิดโรคเรื้อรังต่างๆ และการเปลี่ยนแปลงของฮอร์โมน. นอกจากนี้ภาวะ ED ยังสัมพันธ์กับ คุณภาพการนอน (เช่น ภาวะหยุดหายใจขณะนอนหลับ) และโรคเรื้อรังอื่นๆ เช่น โรคปอด (COPD), โรคต้อหิน, ต่อมลูกหมากโต (BPH) ซึ่งอาจมิใช่สาเหตุโดยตรงแต่เป็นตัวบ่งชี้ว่าผู้ป่วยมีสุขภาพโดยรวมที่ส่งผลต่อสมรรถภาพทางเพศได้ โดยสรุป แพทย์ผู้ดูแลจำเป็นต้องประเมินผู้ป่วย ED ในภาพรวมทั้งร่างกายและจิตใจ เพื่อวินิจฉัยสาเหตุที่แท้จริงและปัจจัยเสี่ยงที่เกี่ยวข้องอย่างครบถ้วน
กลไกทางชีววิทยาและสรีรวิทยาของการแข็งตัวขององคชาต
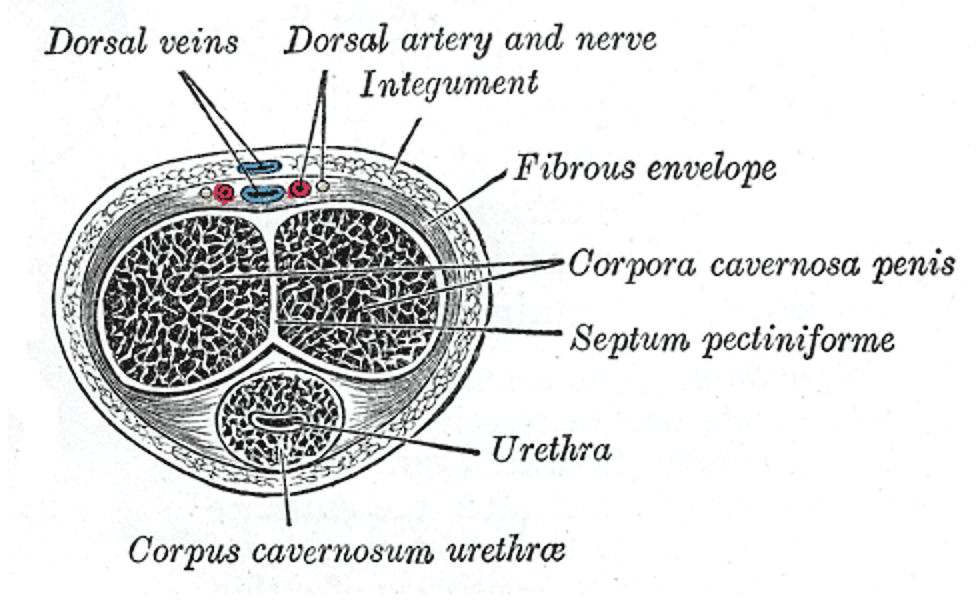
ภาพตัดขวางขององคชาต แสดงโครงสร้างภายใน ได้แก่ คอร์ปอรา คาร์เวอโนซา (Corpora cavernosa; ช่องโพรงฟองน้ำคู่ด้านบน) และคอร์ปัส สปงจิโอซัม (Corpus spongiosum; ช่องโพรงฟองน้ำเดี่ยวด้านล่างที่ล้อมรอบท่อปัสสาวะ). เนื้อเยื่อเหล่านี้เป็นเนื้อเยื่อแข็งตัวที่สามารถกักเก็บเลือด ทำให้องคชาตแข็งตัวเมื่อถูกกระตุ้น
การแข็งตัวขององคชาต (penile erection) เป็นกระบวนการทางชีววิทยาที่สลับซับซ้อน ซึ่งเกี่ยวข้องกับปฏิกิริยาระหว่างระบบประสาท หลอดเลือด และเนื้อเยื่อกล้ามเนื้อเรียบขององคชาต. ภายใต้ภาวะปกติ เมื่อมีสิ่งเร้าทางเพศ (ไม่ว่าจะเป็นสิ่งเร้าทางกาย เช่น การสัมผัส หรือสิ่งเร้าทางจิตใจ เช่น จินตนาการหรือสิ่งกระตุ้นทางสายตา) สมองส่วนไฮโปทาลามัสจะส่งสัญญาณผ่านระบบประสาท พาราซิมพาเทติก (กระซิก) ลงมายังปล้องกระดูกสันหลังระดับ S2-S4 แล้วส่งต่อผ่านเส้นประสาท pelvic splanchnic nerves ไปยังเส้นประสาทโพรงองคชาต (cavernosal nerves) ที่เลี้ยงอวัยวะเพศ เส้นประสาทโพรงนี้หลั่งสารสื่อประสาทสำคัญคือ ไนตริกออกไซด์ (NO) ออกมาที่ปลายประสาท. ไนตริกออกไซด์มีบทบาทเป็น vasodilator ที่กระตุ้นการขยายหลอดเลือดและการคลายตัวของกล้ามเนื้อเรียบภายในโพรงคอร์ปอรา คาร์เวอโนซา (corpora cavernosa) และหลอดเลือดแดงขององคชาต พร้อมกันนั้นเซลล์เยื่อบุผนังหลอดเลือดในโพรงองคชาตก็ปลดปล่อยไนตริกออกไซด์เสริมเข้ามา ซึ่งช่วย คงภาวะการขยายหลอดเลือด ให้ต่อเนื่องหลังจากการเริ่มแข็งตัวโดยประสาท
เมื่อไนตริกออกไซด์แทรกซึมเข้าสู่เซลล์กล้ามเนื้อเรียบ มันจะกระตุ้นเอนไซม์ กวานิลิลไซเคส (guanylyl cyclase) ทำให้ระดับ ไซคลิก GMP (cGMP) ภายในเซลล์สูงขึ้น cGMP ที่เพิ่มขึ้นนี้จะไปกระตุ้นโปรตีนไคเนสชนิด G (PKG) ส่งผลให้ช่องแคลเซียมในเซลล์ปิดลงและช่องโพแทสเซียมเปิดออก เกิดการลดระดับแคลเซียมอิสระภายในเซลล์กล้ามเนื้อเรียบ ระดับแคลเซียมที่ต่ำลงทำให้กล้ามเนื้อเรียบของผนังหลอดเลือดและโพรงคอร์ปอรา คลายตัว อย่างเต็มที่ ส่งผลให้เลือดแดงไหลเข้ามาเติมเต็มโพรงคอร์ปอรา คาร์เวอโนซาทั้งสองจนพองตัว การขยายตัวของโพรงเหล่านี้จะไปกดทับหลอดเลือดดำที่อยู่รอบๆ (subtunical venules) ทำให้เลือดดำไหลออกจากองคชาตได้ลดลงอย่างมาก (veno-occlusive mechanism) ผลลัพธ์คือองคชาตจะแข็งตัวเต็มที่และตึงตัวจนสามารถสอดใส่ได้ โดยมีปริมาณเลือดในองคชาตค้างอยู่สูงสุดและแทบไม่มีเลือดไหลออกจนกว่าจะมีการหลั่งหรือหมดสิ่งเร้าทางเพศ
เมื่อสิ้นสุดการกระตุ้นทางเพศ (เช่น หลังการหลั่งอสุจิ หรือสิ่งเร้าหมดไป) ระบบประสาทซิมพาเทติกจะถูกกระตุ้น นำไปสู่การหลั่งนอร์อีพิเนฟรินที่ทำให้หลอดเลือดหดตัว. ขณะเดียวกันเอนไซม์ ฟอสโฟไดเอสเทอเรส-5 (PDE5) ในเนื้อเยื่อองคชาตจะเริ่มย่อยสลาย cGMP ให้หมดฤทธิ์ลง เมื่อระดับ cGMP ลดต่ำ กล้ามเนื้อเรียบในโพรงองคชาตก็จะหดตัวกลับ หลอดเลือดแดงตีบแคบลง และเลือดส่วนใหญ่ถูกระบายออกทางหลอดเลือดดำ ส่งผลให้องคชาตอ่อนตัวกลับสู่สภาพเดิม จะเห็นได้ว่า กลไกการแข็งตัวขององคชาตต้องอาศัยการทำงานที่ปกติของหลอดเลือดและเส้นประสาท เป็นหลัก ดังนั้นความผิดปกติในกระบวนการใดๆ ไม่ว่าจะเป็นการสร้าง NO ที่ลดลง, การไหลเวียนเลือดที่ไม่เพียงพอ, หรือการรั่วไหลของเลือดดำที่มากผิดปกติ (venous leak) – ล้วนสามารถก่อให้เกิดภาวะ ED ได้ทั้งสิ้น
วิธีการวินิจฉัยและประเมินภาวะ ED
การวินิจฉัยภาวะ ED เริ่มจาก การซักประวัติและตรวจร่างกายอย่างละเอียด โดยแพทย์จะสอบถามทั้งประวัติทางการแพทย์ โรคประจำตัว และประวัติการใช้ยา ตลอดจนรายละเอียดเกี่ยวกับสมรรถภาพทางเพศของผู้ป่วย คำถามสำคัญได้แก่ ระดับความแข็งตัวที่ทำได้ในปัจจุบัน (สามารถสอดใส่ได้หรือไม่), ระยะเวลาที่คงการแข็งตัว, การตื่นตัวตอนเช้า (morning erection) ยังเกิดขึ้นหรือไม่, อาการหลั่งเร็วหรือปัญหาทางเพศอื่นๆ ร่วมด้วยหรือไม่, รวมถึงปัจจัยทางจิตใจและความสัมพันธ์ เช่น ความเครียดหรือความกังวลใจในเรื่องเพศ นอกจากนี้แบบสอบถามมาตรฐานอย่าง ดัชนีชี้วัดสมรรถภาพทางเพศระหว่างประเทศ (International Index of Erectile Function – IIEF) หรือฉบับย่อยที่มี 5 คำถาม (IIEF-5) ถูกนำมาใช้ในการประเมินระดับความรุนแรงของ ED และติดตามผลการรักษาได้อย่างมีประสิทธิภาพ คะแนนจาก IIEF-5 สามารถจัดระดับ ED ได้ตั้งแต่ระดับปกติไปจนถึงรุนแรง และเป็นเครื่องมือที่ผ่านการตรวจสอบความเที่ยงตรงในงานวิจัยนานาชาติ รวมถึงมีฉบับภาษาไทยใช้งานในผู้ป่วยไทยอย่างแพร่หลาย
การตรวจร่างกายควรมุ่งเน้นทั้งระบบหลอดเลือด, ระบบประสาท, ระบบต่อมไร้ท่อ และตรวจอวัยวะเพศอย่างละเอียด แพทย์จะวัดความดันโลหิต ชีพจร และตรวจหัวใจเพื่อหาสัญญาณของโรคหัวใจหรือหลอดเลือด (เนื่องจาก ED อาจเป็นสัญญาณร่วมของโรคเหล่านี้ดังที่กล่าวแล้ว). การตรวจระบบสืบพันธุ์ชายจะประเมินลักษณะองคชาต (มีแผลเป็นหรือความผิดปกติแต่กำเนิดหรือไม่ เช่น โรคเพโรนีย์ที่มีพลักทำให้องคชาตคด), ขนาดและความเรียบตึงของลูกอัณฑะ (เพื่อดูภาวะฮอร์โมนเพศชายต่ำหรือโรคอื่น), และตรวจต่อมลูกหมากทางทวารหนักในผู้ป่วยสูงอายุหรือมีปัจจัยเสี่ยงมะเร็งต่อมลูกหมาก การตรวจระบบประสาทอาจรวมถึงการทดสอบความรู้สึกบริเวณองคชาตและฝีเย็บ (เช่น biothesiometry ใช้การสั่นวัดความรู้สึก) เพื่อคัดกรองปลายประสาทพร่องหน้าที่ในบางราย ทั้งนี้ โดยทั่วไป ยังไม่มีการตรวจทางห้องปฏิบัติการหรือเครื่องมือใดที่จำเป็นอย่างเฉพาะเจาะจงสำหรับ ED ในการประเมินเบื้องต้นทุกราย; การซักประวัติและตรวจร่างกายที่ครอบคลุมมักเพียงพอในการวินิจฉัยสาเหตุส่วนใหญ่ของ ED
อย่างไรก็ตาม การตรวจทางห้องปฏิบัติการพื้นฐาน มักถูกพิจารณาเพื่อค้นหาปัจจัยเสี่ยงที่แก้ไขได้และโรคร่วมที่อาจซ่อนอยู่ โดยทั่วไปแพทย์จะตรวจเลือดเพื่อประเมินระดับน้ำตาลสะสม (HbA1c) เพื่อคัดกรองโรคเบาหวาน, ตรวจไขมันในเลือด (cholesterol profile) สำหรับภาวะไขมันสูง, ตรวจความสมบูรณ์ของไตและตับ (blood urea nitrogen, creatinine, liver enzymes) ในรายที่มีโรคร่วม, ตรวจความสมบูรณ์ของเม็ดเลือด (CBC), และอาจตรวจระดับฮอร์โมน เทสโทสเตอโรนในตอนเช้า ซึ่งเป็นช่วงที่ฮอร์โมนสูงสุด แนวทางสมาคมศัลยแพทย์ระบบทางเดินปัสสาวะสหรัฐฯ (AUA 2018) แนะนำให้ตรวจฮอร์โมนเพศชายอย่างน้อยหนึ่งครั้งในผู้ป่วย ED แต่บางผู้เชี่ยวชาญอาจเลือกตรวจเฉพาะในรายที่สงสัยภาวะพร่องฮอร์โมน (เช่น มีอาการร่วมอย่างความต้องการทางเพศลดลง, อัณฑะฝ่อลีบ) ในกรณีที่ไม่ได้ตรวจในครั้งแรก หากผู้ป่วยรักษาด้วยยา PDE5 inhibitors แล้วไม่ได้ผล ก็ควรตรวจระดับเทสโทสเตอโรนเพิ่มเติมเพื่อดูว่ามีภาวะฮอร์โมนต่ำแฝงอยู่หรือไม่ นอกจากนี้ การตรวจฮอร์โมนอื่นๆ อย่าง LH และโปรแลคติน อาจพิจารณาในรายที่พบฮอร์โมนเพศชายต่ำ เพื่อประเมินความผิดปกติของต่อมใต้สมอง, และตรวจ TSH เพื่อคัดกรองภาวะไทรอยด์ผิดปกติที่อาจมีผลต่อพลังทางเพศ การตรวจปัสสาวะเพื่อดูโรคเบาหวานหรือโปรตีนในปัสสาวะก็อาจทำในบางราย. หากผลตรวจพบความผิดปกติ (เช่น น้ำตาลสูง, ฮอร์โมนต่ำ, ไขมันสูง), ควรส่งรักษาหรือปรึกษาผู้เชี่ยวชาญด้านนั้นๆ ต่อไป เพราะการแก้ไขปัจจัยเหล่านี้อาจช่วยปรับปรุงภาวะ ED ได้
สำหรับ การตรวจพิเศษเพิ่มเติม จะสงวนไว้สำหรับผู้ป่วยรายที่ซับซ้อนหรือรักษาเบื้องต้นแล้วไม่ได้ผล และควรพิจารณาร่วมกับความต้องการของผู้ป่วยอย่างรอบคอบ (เน้นแนวทาง shared decision-making ร่วมกับผู้ป่วยและคู่ครอง) การตรวจเหล่านี้อาจรวมถึง: การตรวจการแข็งตัวขณะหลับ (Nocturnal Penile Tumescence test – NPT) ซึ่งวัดจำนวนและคุณภาพของการแข็งตัวตอนกลางคืนผ่านเครื่องมือ (เช่น RigiScan) – การแข็งตัวตามธรรมชาติขณะหลับมักเกิดในชายสุขภาพดี 3-5 ครั้งต่อคืน การที่ผู้ป่วยยังมีการแข็งตัวเวลากลางคืนปกติบ่งชี้ว่าสรีรวิทยาการแข็งตัวยังทำงานได้ดี สาเหตุ ED ในกรณีนี้อาจเน้นไปทางจิตใจมากกว่า ในทางกลับกัน ถ้าพบความผิดปกติของการแข็งตัวตอนกลางคืน อาจชี้ว่าเป็นสาเหตุทางกาย (เช่น หลอดเลือดหรือประสาทเสียหาย) อย่างไรก็ดี ปัจจุบัน NPT ไม่ได้ใช้เป็นประจำ เนื่องจากความยุ่งยากและมีวิธีอื่นที่เข้าถึงสาเหตุได้ง่ายกว่า การตรวจอัลตราซาวด์ Doppler สีของหลอดเลือดองคชาต หลังฉีดยาขยายหลอดเลือด (เช่น alprostadil) เข้าไปในโพรงองคชาต เพื่อประเมินการไหลเวียนเลือดแดงและการรั่วของเลือดดำ – ค่านี้ช่วยบ่งชี้ว่า ED มีสาเหตุหลักจากหลอดเลือดหรือไม่ โดยค่าความเร็วเลือดในหลอดเลือดแดงโพรงองคชาต (peak systolic velocity) ที่ >35 ซม./วินาทีถือว่าปกติ ในขณะที่ค่าต่ำกว่านั้นอาจบ่งบอกหลอดเลือดตีบ (arteriogenic ED) และหากพบการไหลกลับของเลือดดำเร็ว (end-diastolic velocity สูงเกิน 5 ซม./วินาที) อาจบ่งชี้ภาวะหลอดเลือดดำรั่ว (veno-occlusive dysfunction) การฉีดสารทึบรังสี (Angiography) ในกรณีเฉพาะที่สงสัยการอุดตันของหลอดเลือดแดงองคชาตที่แก้ไขได้ เช่น ผู้ป่วยอายุน้อยที่บาดเจ็บหลอดเลือดไปเลี้ยงองคชาตและพิจารณาผ่าตัดต่อหลอดเลือด; การประเมินทางจิตเวช โดยนักจิตวิทยาหรือจิตแพทย์ ในกรณีที่สงสัยภาวะซึมเศร้าหรือปัญหาทางจิตใจเด่นชัด ซึ่งบางครั้งผู้ป่วยอาจไม่เปิดเผยปัญหาดังกล่าวง่ายๆ จำเป็นต้องใช้การสัมภาษณ์หรือแบบประเมินทางจิตที่เป็นระบบ
โดยสรุป การวินิจฉัย ED ส่วนใหญ่สามารถทำได้จากประวัติและการตรวจพื้นฐาน. การตรวจทางห้องปฏิบัติการช่วยค้นหาปัจจัยเสี่ยงและโรคร่วม ส่วนการตรวจขั้นสูงสงวนไว้สำหรับรายที่ซับซ้อนหรือต้องการวางแผนการรักษาเฉพาะทาง. แนวทางปัจจุบันเน้นให้ ผู้ป่วยมีส่วนร่วมในการตัดสินใจรักษา โดยแพทย์ให้ข้อมูลทางเลือกการรักษาต่างๆ อย่างครบถ้วน แล้วร่วมกันเลือกวิธีที่เหมาะสมกับความต้องการและค่านิยมของผู้ป่วยเป็นสำคัญ เนื่องจากนอกเหนือจากการบำบัดทางจิตใจ (ในกรณี ED ที่เป็นจิตใจล้วนๆ) ยังไม่มีวิธีรักษา ED ทางกายภาพที่ “หายขาด” ได้อย่างถาวรโดยไม่ต้องพึ่งอุปกรณ์หรือยา – การค้นหาสาเหตุเบื้องหลัง ED มีเป้าหมายหลักเพื่อปรับปรุงสุขภาพองค์รวมของผู้ป่วยและคัดกรองโรคอื่น มากกว่าจะเพื่อหาวิธี “รักษาให้หาย” โดยตรง. ดังนั้น หลังการประเมินเบื้องต้นแล้ว สิ่งสำคัญคือการให้ผู้ป่วยได้ลองรักษาวิธีต่างๆ อย่างเหมาะสม จนพบวิธีที่ได้ผลดีและพึงพอใจ
แนวทางการรักษาภาวะ ED
การรักษาภาวะหย่อนสมรรถภาพทางเพศมีหลายวิธี ตั้งแต่การปรับพฤติกรรมและรักษาโรคร่วม, การใช้ยา, การใช้อุปกรณ์ช่วย, การบำบัดทางจิตใจ, จนถึงการผ่าตัด. การเลือกวิธีรักษาที่เหมาะสมควรคำนึงถึงสาเหตุของ ED, ความรุนแรงของอาการ, โรคประจำตัวของผู้ป่วย, และความพึงพอใจของผู้ป่วย/คู่ครอง. โดยทั่วไปสามารถลำดับการรักษาจากวิธีที่มีความรุกรานน้อยไปมาก ดังนี้:
1. การปรับพฤติกรรมและรักษาปัจจัยเสี่ยง: เป็นพื้นฐานสำคัญสำหรับผู้ป่วย ED ทุกราย. การปรับเปลี่ยนวิถีชีวิต ที่ดีต่อสุขภาพช่วยเพิ่มสมรรถภาพทางเพศได้ เช่น การออกกำลังกายสม่ำเสมอ, ควบคุมน้ำหนักให้อยู่ในเกณฑ์, รับประทานอาหารที่มีประโยชน์ (เช่น อาหารเมดิเตอร์เรเนียน), นอนหลับพักผ่อนให้เพียงพอ, งดสูบบุหรี่และสารเสพติด, ลดการดื่มแอลกอฮอล์ (โดยเฉพาะการดื่มหนัก). มีหลักฐานว่าผู้ป่วย ED ที่เป็นโรคอ้วนสามารถฟื้นฟูสมรรถภาพได้บางส่วนหลังลดน้ำหนักและออกกำลังอย่างจริงจัง. นอกจากนี้ การควบคุมโรคเรื้อรังต่างๆ ให้อยู่ในเกณฑ์ดีก็สำคัญมาก เช่น การควบคุมน้ำตาลในผู้ป่วยเบาหวาน, ควบคุมความดันโลหิต, ลดไขมัน LDL ในเลือด, รักษาภาวะฮอร์โมนเพศชายต่ำด้วยการให้ฮอร์โมนทดแทน (ในกรณีที่พิสูจน์แล้วว่ามีระดับฮอร์โมนต่ำและมีอาการสอดคล้อง) เป็นต้น. การปรับปัจจัยเหล่านี้ไม่เพียงช่วยการแข็งตัวโดยตรง แต่ยัง ลดความเสี่ยงโรคหัวใจและหลอดเลือด ในระยะยาวซึ่งเป็นประโยชน์ต่อชีวิตผู้ป่วย
2. การรักษาด้วยยา (Pharmacotherapy): ปัจจุบันยาที่เป็นมาตรฐานอันดับแรกสำหรับ ED คือ ยากลุ่มต้านเอนไซม์ Phosphodiesterase type 5 (PDE-5 inhibitors) ได้แก่ ซิลเดนาฟิล (sildenafil), ทาดาลาฟิล (tadalafil), วาร์เดนาฟิล (vardenafil) และอะวานาฟิล (avanafil). ยากลุ่มนี้ออกฤทธิ์ยับยั้ง PDE5 ซึ่งเป็นเอนไซม์ที่ทำลาย cGMP ในเนื้อเยื่อองคชาต ส่งผลให้ cGMP คงอยู่นานขึ้นและช่วยการคลายตัวของหลอดเลือด/กล้ามเนื้อเรียบในองคชาตได้นานพอที่จะแข็งตัวเต็มที่ ยา PDE5i ไม่สามารถกระตุ้นการแข็งตัวได้เอง แต่ต้องอาศัยสิ่งเร้าทางเพศก่อนเพื่อให้ร่างกายหลั่ง NO เริ่มต้นวงจรการแข็งตัว (ยาเพียงช่วยขยายระยะเวลาการแข็งตัว) ประสิทธิภาพของยากลุ่มนี้สูง โดยมีอัตราความสำเร็จในการมีเพศสัมพันธ์สำเร็จสูงถึง ~76% เมื่อใช้ยาอย่างถูกต้อง และได้ผลในผู้ป่วยหลากหลายสาเหตุ (เช่น ผู้ป่วยเบาหวาน, โรคหัวใจ, ผู้ที่มีภาวะฮอร์โมนต่ำ) ยาแต่ละชนิดมีคุณสมบัติต่างกันไป: ซิลเดนาฟิลและวาร์เดนาฟิลมีระยะออกฤทธิ์ ~4-6 ชม., ทาดาลาฟิลออกฤทธิ์นาน ~24-36 ชม. (จึงบางครั้งเลือกใช้แบบยาประจำวันขนาดต่ำได้), ส่วนอะวานาฟิลมีจุดเด่นคือออกฤทธิ์เร็ว (15-30 นาที) และอาจมีผลข้างเคียงด้านสายตาน้อยกว่า. ผลข้างเคียงทั่วไปของยา PDE5i ได้แก่ ปวดศีรษะ, หน้าแดงร้อน, คัดจมูก, อาหารไม่ย่อย, และบางครั้งมีการเห็นแสงสีฟ้าชั่วคราวในซิลเดนาฟิล ข้อควรระวังคือห้ามใช้ร่วมกับยา ไนเตรต (เช่น ไนโตรกลีเซอรินสำหรับโรคหัวใจ) เนื่องจากอาจทำให้ความดันตกอย่างรุนแรง. นอกจากนี้ควรระวังการใช้ร่วมกับยาขยายหลอดเลือดหรือแอลกอฮอล์ในปริมาณมาก. สำหรับผู้ป่วยที่ใช้ซิลเดนาฟิล ควรทานขณะท้องว่างเพื่อการดูดซึมที่ดี (อาหารไขมันสูงทำให้ยาออกฤทธิ์ช้า) หากผู้ป่วยใช้ยา PDE5 ตัวแรกแล้วไม่ได้ผล ควรลองปรับขนาดหรือเปลี่ยนไปลองยาตัวอื่น เพราะพบว่ามากถึง 50% ของผู้ที่ไม่ตอบสนองต่อยาแรก อาจตอบสนองต่อ PDE5i ตัวที่สอง ในรายที่มีภาวะฮอร์โมนเพศชายต่ำร่วมด้วย การเสริมเทสโทสเตอโรนอาจช่วยเสริมการทำงานของยา PDE5i ให้ได้ผลดีขึ้น แต่ไม่ควรให้ฮอร์โมนเป็นการรักษาเดี่ยวสำหรับ ED หากผู้ป่วยมีฮอร์โมนปกติ
นอกจาก PDE5i ยังมียาชนิดอื่นที่ใช้รักษา ED ในกรณีเฉพาะ. ยาฉีดเข้าอวัยวะเพศชาย (Intracavernosal injection therapy) เป็นวิธีที่มีประสิทธิภาพสูงมาก ใช้ในกรณีที่ยาเม็ดไม่ได้ผลหรือข้อห้าม. ยาที่ใช้ฉีด เช่น ยา Alprostadil (prostaglandin E1) ซึ่งเป็นยาขยายหลอดเลือดที่อนุญาตโดย FDA สำหรับฉีดรักษา ED (นอกจากนี้ยังมีสูตรยาผสมที่ไม่เป็นทางการ เช่น Trimix ซึ่งรวม alprostadil, papaverine และ phentolamine). วิธีนี้ผู้ป่วยต้องฉีดยาเข้าที่โพรงคอร์ปอรา คาร์เวอโนซาขององคชาตเองก่อนมีเพศสัมพันธ์ประมาณ 5-15 นาที. อัตราความสำเร็จของการรักษาด้วยยาฉีดถือว่าสูงมาก – รายงานบางฉบับระบุว่าสามารถทำให้องคชาตแข็งตัวได้เพียงพอใน ถึง ~94% ของผู้ป่วย – จึงเป็นทางเลือกที่สำคัญเมื่อยาเม็ดใช้ไม่ได้ผล. อย่างไรก็ตาม ข้อจำกัดของวิธีนี้คือความไม่สะดวกและความเจ็บปวดจากการฉีด ทำให้ผู้ป่วยบางรายยอมรับได้ยาก. ผลข้างเคียงที่อาจเกิดขึ้น ได้แก่ อาการปวดหรือแสบร้อนที่องคชาตขณะยาออกฤทธิ์ (พบได้บ่อยใน alprostadil), ภาวะองคชาตแข็งตัวค้างนานผิดปกติ (priapism) ซึ่งแม้พบไม่บ่อยนักแต่ถือเป็นภาวะฉุกเฉินที่ต้องรักษาทันที (ความเสี่ยง priapism จากยาฉีดคิดเป็นราว 8.8% ของเคส priapism ทั้งหมด) และอาจมีพังผืดหรือแผลเป็นในเนื้อเยื่อองคชาตหากฉีดบ่อยๆ. ผู้ป่วยที่ใช้วิธีนี้ควรได้รับการฝึกฝนวิธีฉีดและขนาดยาที่เหมาะสมจากแพทย์ รวมถึงคำแนะนำให้รีบไปโรงพยาบาลหากแข็งตัวนานเกิน 4 ชั่วโมง เพื่อป้องกันความเสียหายถาวรต่อเนื้อเยื่อ ยา Alprostadil ยังมีรูปแบบ ยาเหน็บท่อปัสสาวะ (Intraurethral suppository) ขนาดเล็ก (ชื่อทางการค้า MUSE) ที่ผู้ป่วยสามารถสอดเข้าทางท่อปัสสาวะเพื่อดูดซึมสู่เนื้อเยื่อโพรงองคชาต แต่ประสิทธิภาพต่ำกว่าการฉีดและอาจทำให้แสบท่อปัสสาวะได้
3. การใช้อุปกรณ์ช่วย: อุปกรณ์สุญญากาศ (Vacuum erectile device – VED) เป็นทางเลือกที่ไม่ต้องใช้ยาและไม่ผ่าตัด โดยใช้หลักการสร้างแรงดูดสุญญากาศรอบองคชาตเพื่อดึงเลือดเข้าไปในโพรงคอร์ปอรา คาร์เวอโนซา แล้วใช้ห่วงยางรัดโคนองคชาตไว้เพื่อกันเลือดไหลย้อนกลับ. ผู้ป่วยสามารถใช้อุปกรณ์นี้ก่อนมีกิจกรรมทางเพศ โดยให้องคชาตแข็งตัวค้างไว้ได้ประมาณ 30 นาทีเมื่อรัดห่วงที่โคนไว้ การใช้งานต้องอาศัยการฝึกฝนและความคุ้นเคย แต่เมื่อใช้อย่างถูกต้องอุปกรณ์นี้มี ประสิทธิภาพค่อนข้างสูง – รายงานประสิทธิผลโดยรวมประมาณ 70% และบางการศึกษาที่ให้การสอนและติดตามอย่างดีพบว่าสามารถทำให้องคชาตแข็งตัวได้สำเร็จถึง ~94% ของกรณี ข้อดีคือหลีกเลี่ยงผลข้างเคียงทางระบบของยาและสามารถใช้ได้บ่อยเท่าที่ต้องการ. ข้อจำกัดคือบางคู่รู้สึกว่าไม่เป็นธรรมชาติหรือยุ่งยากในการเตรียมอุปกรณ์ และอาจมีอาการชาหรืออวัยวะเย็นจากการรัด. โดยรวมแล้ว VED ถือเป็นวิธีที่ปลอดภัยและคุ้มค่า สามารถใช้เป็นการรักษาระยะยาวได้หากผู้ป่วยพึงพอใจ
4. การบำบัดทางจิตใจและการปรึกษาคู่สมรส: ในผู้ป่วยที่มีองค์ประกอบทางจิตใจเกี่ยวข้อง การทำ จิตบำบัดหรือนักบำบัดทางเพศ (sex therapy) จะช่วยแก้ไขวงจรความวิตกกังวล–ความล้มเหลวซ้ำซ้อนที่เกิดขึ้น. เทคนิคการบำบัดเช่น Sensate focus (ฝึกการสัมผัสและสร้างความไว้วางใจโดยไม่เน้นการสอดใส่) และการปรับความคิดเรื่องเพศให้ถูกต้อง (cognitive restructuring) สามารถลดความกังวลและเพิ่มความเชื่อมั่นให้ผู้ป่วยได้. การมี คู่สมรสหรือคู่นอนเข้าร่วมในการบำบัด ก็เป็นปัจจัยสำคัญ เพราะ ED มักส่งผลกระทบต่อทั้งสองฝ่าย การสื่อสารที่เปิดเผยและการทำความเข้าใจร่วมกันจะช่วยฟื้นฟูความสนิทสนมและลดแรงกดดันในการมีเพศสัมพันธ์. ในกรณีผู้ป่วยมีโรคทางจิตเวชชัดเจน เช่น ซึมเศร้าหรือวิตกกังวลรุนแรง ควรให้การรักษาจิตเวชควบคู่ไป (อาจต้องปรับยาโรคซึมเศร้าให้ไม่มีผลต่อการแข็งตัวมากเกินไป). การบำบัดทางจิตใจมักได้ผลดีใน ED สาเหตุจิตใจหรือกลุ่มวัยหนุ่ม และอาจใช้ร่วมกับการรักษาทางกาย (เช่น ยา) เพื่อเพิ่มความสำเร็จ
5. การผ่าตัดฝังแกนอวัยวะเพศ (Penile prosthesis): ถือเป็นทางเลือกสุดท้ายสำหรับผู้ป่วยที่รักษาด้วยวิธีข้างต้นทั้งหมดแล้วไม่ได้ผลหรือไม่สามารถใช้วิธีอื่น และยังมีความต้องการที่จะมีเพศสัมพันธ์อย่างต่อเนื่อง. การผ่าตัดนี้จะใส่อุปกรณ์เทียมเข้าไปในองคชาต – ปัจจุบันมีสองชนิดหลักคือ ชนิดกึ่งแข็งตัว (malleable/semi-rigid rods) ซึ่งเป็นแกนซิลิโคนคู่ที่ดัดให้อ่อนหรือตั้งขึ้นได้ตามต้องการ, และ ชนิดสูบได้ (inflatable prosthesis) ซึ่งประกอบด้วยกระบอกสูบคู่ในโพรงองคชาต ต่อกับปั๊มที่ฝังในถุงอัณฑะและแทงก์น้ำเกลือในช่องท้อง ผู้ป่วยสามารถกดปั๊มเพื่อส่งน้ำเกลือเข้าไปในกระบอกสูบทำให้องคชาตแข็งตัว และกดวาล์วปล่อยน้ำให้ยุบเมื่อเสร็จกิจกรรม. การฝังแกนอวัยวะเพศมี อัตราความสำเร็จและความพึงพอใจสูงมาก – เกือบทุกกรณีที่ผ่าตัดสามารถใช้งานได้ผล และแบบสำรวจพบว่าผู้ป่วยและคู่ครองมีความพึงพอใจต่อผลลัพธ์โดยรวมสูงกว่า 90% เนื่องจากช่วยให้กลับมามีเพศสัมพันธ์ได้ใกล้เคียงปกติที่สุด ความเสี่ยงของการผ่าตัดนี้ได้แก่ ภาวะติดเชื้อ (ประมาณ <3%), การทำงานผิดปกติของอุปกรณ์ในระยะยาว (5-10% ใน 10 ปีแรก อาจต้องผ่าตัดแก้ไขหรือเปลี่ยนอุปกรณ์) และการบาดเจ็บต่อเนื้อเยื่อรอบข้าง. หลังผ่าตัดผู้ป่วยจะสูญเสียกลไกการแข็งตัวตามธรรมชาติไป (เนื่องจากเนื้อเยื่อแข็งตัวเดิมถูกแทนที่ด้วยแกนเทียม) แต่ในกรณีที่วิธีอื่นใช้ไม่ได้ ผลลัพธ์ที่ได้จากการฝังแกนถือว่าคุ้มค่า. การผ่าตัดนี้ควรทำโดยศัลยแพทย์ทางเดินปัสสาวะที่มีความชำนาญและต้องมีการปรึกษาให้ข้อมูลผู้ป่วยอย่างละเอียดก่อนตัดสินใจ
6. การรักษาอื่นๆ: ในบางกรณีเฉพาะหรือระยะแรกของชีวิตคู่ แพทย์อาจแนะนำ การปรับกิจกรรมทางเพศ เช่น การเปลี่ยนเวลา/สถานที่ลดความกังวล, การใช้สารหล่อลื่นช่วยลดความเจ็บปวด, การสำเร็จความใคร่ด้วยตนเองก่อนเพื่อลดความตื่นเต้นเกินไป เป็นต้น. นอกจากนี้ยังมี ยาทางเลือกและอาหารเสริมบางชนิด ที่ถูกกล่าวอ้างว่าช่วยสมรรถภาพ เช่น โสม, L-arginine, โยฮิมบีน เป็นต้น แต่หลักฐานทางการแพทย์ยังจำกัดและควรใช้อย่างระมัดระวังโดยปรึกษาแพทย์.
โดยสรุป ปัจจุบัน ผู้ป่วย ED แทบทุกรายสามารถรักษาได้ด้วยวิธีใดวิธีหนึ่ง ในข้างต้นอย่างสำเร็จ แนวทางคือเริ่มจากวิธีง่ายและปลอดภัยก่อน แล้วไล่ระดับไปจนถึงการผ่าตัดหากจำเป็น. การรักษาหลายวิธีสามารถใช้ร่วมกันเพื่อเสริมประสิทธิภาพ เช่น การทานยา PDE5i ร่วมกับใช้เครื่องสุญญากาศ หรือการฉีดยาร่วมกับกินยา เป็นต้นการเปิดใจพูดคุยกับแพทย์และคู่ครอง รวมถึงการลองปรับใช้วิธีต่างๆ อย่างเหมาะสม จะช่วยให้ผู้ป่วยพบแนวทางที่ได้ผลและมีชีวิตทางเพศที่มีคุณภาพได้อีกครั้ง
ผลกระทบทางจิตใจและคุณภาพชีวิตของผู้ป่วย
ภาวะ ED ส่งผลกระทบกว้างขวางต่อด้านจิตใจ อารมณ์ และคุณภาพชีวิตของทั้งผู้ป่วยและคู่ครอง. ผู้ชายหลายคนมองว่าสมรรถภาพทางเพศเป็นส่วนหนึ่งของความภาคภูมิใจและบทบาทความเป็นชาย การที่ไม่สามารถแข็งตัวได้อาจทำให้รู้สึกสูญเสียคุณค่าในตัวเองและเกิด ความรู้สึกล้มเหลว. ผู้ป่วยมักเกิดความวิตกกังวลว่าจะทำให้คู่ครองผิดหวัง และยิ่งพยายามมากก็ยิ่งกดดันตัวเอง เกิดเป็นวงจร anxiety–failure ที่ทำให้อาการแย่ลง. หลายคนอาจหลีกเลี่ยงความสัมพันธ์ทางเพศหรือแสดงท่าทีเย็นชาต่อคู่ครองเพราะกลัวเผชิญกับความล้มเหลว นำไปสู่ ความตึงเครียดในความสัมพันธ์ หรือปัญหาครอบครัวตามมา. ผู้ป่วย ED จำนวนไม่น้อยพัฒนาภาวะซึมเศร้าตามหลัง เพราะรู้สึกสิ้นหวังกับสภาพของตนเอง และการมี ED ยังสัมพันธ์กับอัตราการเกิดภาวะซึมเศร้าและวิตกกังวลสูงขึ้นเมื่อเทียบกับคนทั่วไป
งานวิจัยชี้ว่าแม้ ED จะไม่ได้เกิดจากปัญหาทางจิตใจโดยตรงเป็นส่วนใหญ่ แต่ การมี ED เองสามารถทำให้เกิดปัญหาทางจิตใจตามมา อย่างเด่นชัด – เช่น ทำให้ความมั่นใจในตนเองลดลง, เพิ่มความเครียดและความวิตกกังวล, และบั่นทอนสายสัมพันธ์กับคู่ครอง ผลกระทบเหล่านี้อาจส่งต่อไปยังชีวิตประจำวัน เช่น มีสมาธิในการทำงานลดลง หลีกเลี่ยงกิจกรรมสังคมเพราะอับอาย หรือรู้สึกโดดเดี่ยว. นอกจากนี้คู่ครองของผู้ป่วย ED ก็ได้รับผลกระทบทางจิตใจเช่นกัน หลายคนอาจเข้าใจผิดว่าตนเองไม่น่าดึงดูดอีกต่อไปหรือรู้สึกโกรธ/เศร้าที่ความสัมพันธ์เปลี่ยนไป. ED จึงถือเป็น ปัญหาสุขภาพที่กระทบคุณภาพชีวิต ในระดับใกล้เคียงกับโรคเรื้อรังอื่นๆ อย่างเบาหวานหรือข้ออักเสบ เมื่อพิจารณาถึงความทุกข์ที่เกิดขึ้นกับทั้งผู้ป่วยและคู่ครอง
การจัดการผลกระทบทางจิตใจเหล่านี้เป็นส่วนสำคัญของการดูแลผู้ป่วย ED. การให้คำปรึกษาและสนับสนุนด้านจิตใจ ควรมาควบคู่กับการรักษาทางกายภาพ. แพทย์ควรอธิบายให้ผู้ป่วยเข้าใจว่า ED เป็นภาวะที่รักษาได้และพบได้บ่อย เพื่อคลายความอับอายและความรู้สึกโดดเดี่ยว. การเชิญคู่ครองเข้ามามีส่วนร่วมในการพูดคุยก็ช่วยให้ทั้งสองฝ่ายเปิดใจเข้าใจกัน ลดความตึงเครียดและความเข้าใจผิด. ในบางรายที่มีภาวะซึมเศร้าหรือวิตกกังวลเด่นชัด อาจต้องใช้ยาและการบำบัดทางจิตเวชร่วมด้วย. เมื่อการรักษา ED ประสบผลสำเร็จ มักพบว่าสภาวะทางอารมณ์และความสัมพันธ์ของผู้ป่วยดีขึ้นอย่างชัดเจน – ความมั่นใจกลับมา ความพึงพอใจในชีวิตคู่เพิ่มขึ้น ส่งผลให้คุณภาพชีวิตโดยรวมของผู้ป่วยสูงขึ้นตามลำดับ. หากแม้การรักษาทางกายยังไม่เห็นผลทันที การได้รับความเข้าใจและสนับสนุนทางใจจากคู่ครองและผู้เชี่ยวชาญก็สามารถช่วยผู้ป่วยรับมือกับปัญหาได้ดียิ่งขึ้น ลดผลกระทบด้านลบที่มีต่อชีวิตลงได้
แนวโน้มงานวิจัยและนวัตกรรมในการรักษา ED ในปัจจุบัน
ปัจจุบันมีความพยายามในการพัฒนาแนวทางการรักษา ED รูปแบบใหม่ๆ ที่มุ่งเน้นการฟื้นฟูกลไกการแข็งตัวตามธรรมชาติโดยตรง และลดความจำเป็นในการใช้ยาหรืออุปกรณ์ในระยะยาว. นวัตกรรมเด่นๆ และแนวโน้มงานวิจัยล่าสุด ได้แก่:
-
การรักษาด้วยคลื่นเสียงความถี่ต่ำ (Low-Intensity Extracorporeal Shockwave Therapy – Li-ESWT): เป็นเทคนิคใหม่ที่ไม่รุกราน ซึ่งใช้คลื่นเสียงพลังงานต่ำยิงไปยังเนื้อเยื่อองคชาตเพื่อกระตุ้นการสร้างหลอดเลือดใหม่ (neovascularization) และฟื้นฟูการทำงานของเยื่อบุหลอดเลือด. แนวคิดคือการรักษาที่ต้นเหตุในผู้ป่วย ED ชนิดหลอดเลือด (เช่น จากเบาหวานหรือความดันโลหิตสูง) แทนที่จะใช้ยาเฉพาะกิจ. มีงานวิจัยแบบสุ่มที่มีกลุ่มควบคุมหลอก (sham-controlled RCT) แสดงให้เห็นว่า Li-ESWT สามารถ เพิ่มคะแนนความแข็งตัว (เช่น IIEF หรือ SHIM) ได้อย่างมีนัยสำคัญเมื่อเทียบกับกลุ่มควบคุม และผลที่ได้คงอยู่ยาวนานถึง 1-2 ปีหลังการรักษา ผู้ป่วยจำนวนหนึ่งสามารถกลับมามีการแข็งตัวที่เพียงพอโดยไม่ต้องพึ่งยาในช่วงเวลาดังกล่าว. อย่างไรก็ดี ประสิทธิผลในระยะยาวเกินกว่า 2 ปีดูเหมือนจะลดลง และอาจต้องมีการรักษาซ้ำ. Li-ESWT ยังถือเป็นวิธีใหม่ที่อยู่ในขั้นประเมินผล – แม้ผลการศึกษาส่วนใหญ่จะเป็นบวกและไม่มีผลข้างเคียงร้ายแรง แต่ยังต้องมีการวิจัยเพิ่มเกี่ยวกับเกณฑ์ผู้ป่วยที่เหมาะสม, ปริมาณพลังงานที่ใช้, และระยะเวลาผลลัพธ์. หลายประเทศ (รวมถึงประเทศไทยในบางศูนย์) เริ่มมีการให้บริการ Li-ESWT สำหรับ ED ในผู้ป่วยที่ไม่ตอบสนองต่อยา โดยถือเป็น ทางเลือกเสริม นอกเหนือการรักษามาตรฐาน
-
การบำบัดด้วยเซลล์ต้นกำเนิด (Stem cell therapy): เป็นแขนงของการแพทย์ฟื้นฟู (regenerative medicine) ที่มีศักยภาพน่าสนใจสำหรับ ED. การใช้ เซลล์ต้นกำเนิดมีเซนไคม์ (mesenchymal stem cells) เช่น เซลล์ต้นกำเนิดจากไขมัน (Adipose-derived stem cells – ADSC) หรือจากไขกระดูก นำมาฉีดเข้าที่องคชาต สามารถช่วยซ่อมแซมเนื้อเยื่อที่เสียหาย กระตุ้นการสร้างหลอดเลือดใหม่ และเพิ่มจำนวนเซลล์กล้ามเนื้อเรียบในโพรงองคชาตตามงานวิจัยสัตว์ทดลอง. การศึกษาระยะเริ่มต้นในมนุษย์มีรายงานผลในเชิงบวกบางส่วน – เช่น meta-analysis หนึ่งพบว่าการใช้ ADSC ในสัตว์ทดลองช่วยฟื้นฟูการแข็งตัวได้จริงโดยมีการสร้างเนื้อเยื่อใหม่ในโพรงองคชาตที่ถูกทำลาย มีการทดลองทางคลินิกขนาดเล็กที่ฉีดเซลล์ต้นกำเนิดเข้าสู่เนื้อเยื่อองคชาตผู้ป่วย ED ที่ไม่ตอบสนองต่อยา พบว่าหลังการฉีดผู้ป่วยบางรายมีคะแนน IIEF ดีขึ้นและสามารถมีเพศสัมพันธ์ได้. อย่างไรก็ตาม การบำบัดนี้ยังอยู่ในขั้นวิจัยทดลอง (Phase I/II) และต้องการข้อมูลด้านความปลอดภัยและประสิทธิผลในระยะยาว. ประเด็นที่ต้องศึกษาเพิ่มเติม ได้แก่ ปริมาณเซลล์ที่เหมาะสม, ชนิดเซลล์ที่ให้ผลดีที่สุด, ความจำเป็นต้องกระตุ้นเซลล์ก่อนฉีดหรือไม่, และความถี่ในการรักษา. นับถึงปัจจุบัน ยังไม่มีการรักษา ED ด้วยสเต็มเซลล์ที่ผ่านการรับรองสำหรับใช้งานทั่วไป แต่ศักยภาพในระยะยาวคือการทำให้เนื้อเยื่อองคชาตที่เสื่อมสามารถฟื้นตัว จนอาจไม่ต้องพึ่งยา
-
การฉีดพลาสมาที่มีเกล็ดเลือดเข้มข้น (Platelet-Rich Plasma – PRP): วิธีนี้นำเลือดผู้ป่วยมาปั่นแยกให้ได้พลาสมาที่อุดมด้วยเกล็ดเลือดและสารกระตุ้นการเจริญเติบโตต่างๆ แล้วฉีดกลับเข้าไปที่องคชาต. แนวคิดคือ PRP อาจช่วยซ่อมแซมหลอดเลือดและเนื้อเยื่อคล้ายกับเซลล์ต้นกำเนิดแต่ใช้วัตถุดิบจากตัวผู้ป่วยเอง. PRP ได้รับความนิยมในเชิงการตลาด (รู้จักกันในชื่อ “P-Shot”) และมีคลินิกเอกชนหลายแห่งโฆษณาว่าสามารถเพิ่มสมรรถภาพทางเพศได้. อย่างไรก็ดี หลักฐานทางวิทยาศาสตร์ในปัจจุบันยังไม่ชัดเจน – รายงานการศึกษาทางคลินิกยังมีจำกัดและผลลัพธ์ที่ได้มีความหลากหลาย. บางงานพบว่าผู้ป่วยมี IIEF ดีขึ้นเล็กน้อยหลังฉีด PRP แต่การศึกษาเหล่านี้มักไม่มีการเปรียบเทียบกับกลุ่มควบคุมที่เหมาะสม. คณะผู้เชี่ยวชาญระบบทางเดินปัสสาวะส่วนใหญ่ยัง ไม่รับรอง PRP เป็นมาตรฐานการรักษา ED โดยชี้ว่าหลักฐานยังอ่อนและจำเป็นต้องวิจัยเพิ่มเติม ดังนั้น PRP จึงควรถูกจัดอยู่ในข่ายการรักษาเชิงทดลองเท่านั้นในขณะนี้
-
การรักษาด้วยยีน (Gene therapy): อีกแนวทางหนึ่งที่อยู่ระหว่างการพัฒนาคือการนำยีนเข้าไปแก้ไขหรือเสริมการทำงานของเซลล์ในองคชาตที่มีปัญหา. ตัวอย่างที่มีการทดลองแล้ว ได้แก่ ยีน hMaxi-K ซึ่งเป็นยีนที่ควบคุมการสร้างช่องโปรตีนโพแทสเซียม (BK_{Ca} channel) ในกล้ามเนื้อเรียบของหลอดเลือด. การแสดงออกของยีนนี้ช่วยให้กล้ามเนื้อเรียบคลายตัวได้ง่ายขึ้นและหลอดเลือดขยายตัวดีขึ้น. ในการทดลองระยะที่ 1 กับผู้ป่วย ED ที่ไม่ตอบสนองต่อยา 11 ราย นักวิจัยได้ฉีด DNA เปลือย (plasmid) ที่มียีน hMaxi-K เข้าสู่โพรงองคชาตของผู้ป่วย พบว่าผู้ป่วยกลุ่มที่ได้รับขนาดยาสูงบางรายมีการแข็งตัวที่ดีขึ้นอย่างชัดเจนและต่อเนื่องนานหลายเดือน โดยไม่ต้องใช้ยา PDE5 เพิ่มเติม ทั้งยังไม่พบผลข้างเคียงรุนแรงจากการรักษา นี่เป็นสัญญาณว่า gene therapy อาจเป็นหนทางในอนาคตที่ให้ผลระยะยาวและลดการพึ่งพาการใช้ยาเฉพาะกิจ. ปัจจุบัน gene therapy สำหรับ ED ยังอยู่ในขั้นทดลองระยะต้นเท่านั้น แต่มีความก้าวหน้ามากขึ้นเรื่อยๆ. มีการศึกษายีนเป้าหมายอื่นๆ เช่น ยีนที่กระตุ้นการสร้าง ไนตริกออกไซด์ซินเทส (NOS), ยีนที่ยับยั้งการทำงานของ TGF-β_1 (ที่ทำให้เกิดพังผืดในองคชาต) เป็นต้น. หากเทคโนโลยีนี้พัฒนาสำเร็จ วันข้างหน้าแพทย์อาจสามารถฉีดยีนหรือโมเลกุลเล็กๆ เข้าไปที่องคชาตเพื่อแก้ไขความผิดปกติในระดับเซลล์ ซึ่งจะเป็นการรักษาที่ตรงจุดและยั่งยืนยิ่งขึ้น
-
ยาและเทคโนโลยีใหม่อื่นๆ: นอกจากแนวทางข้างต้น ยังมีการวิจัยยาและอุปกรณ์ใหม่ๆ สำหรับ ED อย่างต่อเนื่อง. ตัวอย่างเช่น การพัฒนายาในกลุ่ม สารกระตุ้น Guanylate cyclase (sGC stimulators) ซึ่งออกฤทธิ์เพิ่ม cGMP โดยตรง (ไม่ผ่าน NO) อาจมีประโยชน์ในผู้ป่วยที่กลไก NO เสียไป (มียา riociguat ที่ใช้รักษาปอดตันเรื้อรังอยู่ และอยู่ระหว่างทดลองใน ED), ยากลุ่มตัวรับเมลาโนคอร์ติน (เช่น PT-141 หรือ Bremelanotide) ที่ออกฤทธิ์ผ่านระบบประสาทส่วนกลางเพื่อเพิ่มความต้องการทางเพศและช่วยการแข็งตัว (ปัจจุบันอนุมัติสำหรับรักษาภาวะความต้องการทางเพศต่ำในสตรี แต่มีการศึกษานำมาใช้ในชายที่มี ED), นอกจากนี้ การออกแบบแกนอวัยวะเพศเทียมรุ่นใหม่ ที่บางลง ประสิทธิภาพสูงขึ้น หรือติดตั้งด้วยรีโมทควบคุมไร้สาย ก็มีการพัฒนาเพื่อลดปัญหาของรุ่นเก่า. ยังมีแนวคิดใช้ การกระตุ้นประสาทไฟฟ้า (neurostimulation) เช่น กระตุ้นเส้นประสาทกระเบนเหน็บ (sacral nerve) หรือเส้นประสาทดอร์ซัลขององคชาต เพื่อส่งเสริมการแข็งตัวในผู้ที่มีความเสียหายทางประสาท
กล่าวโดยสรุป แนวโน้มอนาคตในการรักษา ED กำลังมุ่งไปสู่แนวทางที่ รักษาต้นเหตุเชิงการทำงานของเนื้อเยื่อ มากขึ้น แทนที่จะเป็นการรักษาปลายเหตุเฉพาะกิจ. เป้าหมายคือการฟื้นฟูความสามารถในการแข็งตัวอย่างเป็นธรรมชาติ ลดการพึ่งพายาและเพิ่มความเป็นอิสระให้ผู้ป่วย. แม้งานวิจัยหลายด้านยังอยู่ในขั้นทดลองและต้องการเวลาสะสมหลักฐาน แต่ความก้าวหน้าเหล่านี้สร้างความหวังว่าในอนาคต ผู้ป่วย ED จะมีทางเลือกในการรักษาที่หลากหลายและมีประสิทธิภาพยิ่งขึ้น อันจะนำไปสู่การยกระดับคุณภาพชีวิตของผู้ชายที่ประสบภาวะนี้ทั่วโลก.
แหล่งอ้างอิง:
-
Bumrungrad Hospital. การหย่อนสมรรถภาพทางเพศ (Erectile Dysfunction)
-
StatPearls – Erectile Dysfunction (2023). [NCBI Bookshelf] – Prevalence and age-related incidence Global prevalence Pathophysiology of erection, PDE5 inhibitors efficacy , etc.
-
International Journal of Impotence Research (2019). Hui J et al. Trends in erectile dysfunction research 2008-2018. – Quote: “By the year 2025, the number of ED cases worldwide is expected to reach 322 million.”
-
StatPearls – ED (2023). Etiology and Cardiovascular link. – ED precedes coronary disease by years ; 50% of CAD patients have ED ED increases CV risk
-
Advances in Urology (2022). Stem cell therapy for ED. – Table of ED causes: vascular, neuro, hormonal, medication, etc
-
StatPearls – ED (2023). Psychological impact. – ED damages relationships, causes anxiety and low self-esteem
-
Asian Journal of Andrology (2024). Shockwave therapy RCT. – Li-ESWT improved erectile function at 1-2 years post-treatment
-
Frontiers in Medicine (2023). Stem cell therapy review. – ADSC meta-analysis shows regeneration of erectile tissue
-
Cleveland Clinic / JWatch (2021). PRP for ED. – Insufficient evidence for PRP effectiveness
-
ScienceDaily (2006). Gene therapy for ED trial. – hMaxi-K gene therapy showed sustained improvement in some patients, potentially obviating on-demand meds

